Новая мишень для противораковых препаратов: ученые нашли «ахиллесову пяту» рецептора HER3
Опубликовано lana в 17 июня, 2011 - 21:00
Одним из отличительных признаков раковых клеток
является неконтролируемый рост, провоцируемый молекулярными сигналами,
которые заставляют клетки продолжать деление. Ученые Массачусетского
технологического института (Massachusetts Institute of Technology, MIT) и
больницы Brigham and Women’s Hospital нашли новый способ блокирования
одного из белков, передающих подобные сигналы – рецептора, известного как HER3.
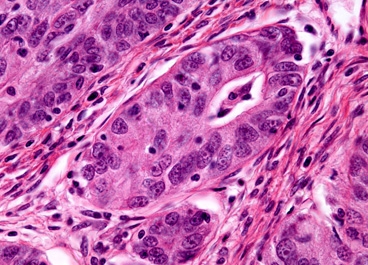 Микроскопическое изображение аденокарциномы яичников. Микроскопическое изображение аденокарциномы яичников.
Ученые MIT нашли новый способ нарушить функцию белка
HER3, часто гиперэкспрессируемого опухолями яичников.
(Фото: Nikon микроскопия)
Лекарственные вещества, нарушающие функцию близких «родственников» рецептора HER3, рецепторов EGFR и HER2,
уже доказали свою эффективность в лечении многих типов рака, и в
настоящее время проводятся клинические испытания антител, направленных
против рецептора HER3. Этот рецептор представляет огромный интерес для
изучающих рак биологов, так как, как правило, вовлечен в развитие двух
из самых опасных форм этого заболевания – рака яичников и поджелудочной
железы.
Исследование, опубликованное в журнале Journal of Biological Chemistry, началось со случайного открытия, сделанного в ходе реализации проекта в области регенеративной медицины. Его соавтор Луис Альварес (Luis Alvarez) заинтересовался регенеративной медициной потому, что знал многих солдат, раненных в Ираке и Афганистане.
В поисках путей стимуляции восстановления костной ткани Альварес
разработал серию парных белков, которые, как считают ученые, могут
способствовать взаимодействию между рецепторами роста, такими как HER3 и
EGFR, и регулировать рост и дифференциацию клеток кости.
Разработанные Альваресом белки оказывают определенное воздействие на
регенерацию, но ученые заметили, что в некоторых случаях они
останавливают рост клеток и их миграцию. Альварес и другие ученые из
лаборатории профессора Школы инженерии Отделения биологической инженерии
MIT Линды Гриффит (Linda Griffith) решили проверить,
что произойдет, если таким белком обработать раковые клетки. К их
удивлению они обнаружили, что клетки останавливали рост и в некоторых
случаях умирали.
«Это было совсем не то, чего мы ожидали – трудно представить, что
можно выключить рецептор чем-то, что обычно активирует его», –
комментирует неожиданные результаты профессор Гриффит. «Мы занялись этим
только потому, что в нашей лаборатории есть сотрудники, работающие с
раковыми клетками, и мы подумали: «Если это оказывает эффект на
стволовые клетки, давайте просто попробуем это на опухолевых клетках и
посмотрим, не произойдет ли чего-либо интересного»».
Примерно в то же время у профессора Гриффит тоже появился личный
интерес к этому семейству клеточных рецепторов: у нее была
диагностирована форма рака молочной железы, при которой часто
гиперэкспрессируется рецептор EGFR.
Биологи уделяют много внимания рецептору EGFR – он является мишенью противораковых препаратов Эрбитукс (Erbitux), Иресса (Iressa) и Тарцева
(Tarceva). Но не все типы рака с гиперэкспрессией рецепторов EGFR
отвечают на адресную терапию. Действие первого весьма успешного
адресного химиотерапевтического препарата Герцептина (Herceptin) направлено на другой рецептор этого семейства – HER2.
Полученный в MIT новый белок имеет своей мишенью специфическую
особенность рецептора HER3, которая в данном случае оказалась его
«ахиллесовой пятой»: чтобы передать свои стимулирующие рост сигналы HER3
должен работать в тандеме с другим рецептором, как правило, HER2.
Новый белок, состоящий из двух молекул белка нейрегулина
(neuregulin), нарушает это взаимодействие. Одна молекула нейрегулина
обычно стимулирует рецептор HER3, способствуя росту и дифференциации
клеток. Однако если клетки получают спаренный нейрегулин, последний
связывает два соседних рецептора HER3, предотвращая их взаимодействие с
рецепторами HER2, которое необходимо для передачи сигналов.
Ученые протестировали действие спаренной молекулы нейрегулина на
шести различных типах раковых клеток, гиперэкспрессирующих HER3, и
обнаружили, что она эффективно подавляет рост всех из них, включая тип
клеток, резистентный к препаратам, мишенью которых является
рецептор EGFR.
Профессор онкологии Калифорнийского университета в Сан-Франциско (University of California at San Francisco), Марк Моассер
(Mark Moasser), не принимавший участия в этой работе, считает новый
подход умным и изящным, хотя, чтобы определить, будет ли он эффективен
на живых организмах, необходимо продолжение исследований. «Базируясь на
этом механизме, метод имеет мощный потенциал и закладывает основу для
будущей большой работы», – комментирует ученый результаты экспериментов.
Сейчас ученые MIT и больницы Brigham and Women’s Hospital работают
над новой версией молекулы, которая больше подойдет для экспериментов на
живых организмах. В их планах – начать ее тестирование в
ближайшее время.
Аннотация к статье
Engineered bivalent ligands to bias ErbB receptor-mediated signaling and phenotypes
- Источник(и):
LifeSciencesToday http://web.mit.edu/…ls-0608.html
http://www.nanonewsnet.ru/ne
|









