Чем меньше наночастицы, тем больше выход реакции
Опубликовано ssu-filippov в 19 января, 2011 - 02:44
 Высокий выход целевого продукта может обуславливать применение метода в промышленности. (Рисунок из Science, 2011). Высокий выход целевого продукта может обуславливать применение метода в промышленности. (Рисунок из Science, 2011).
Исследователи разработали катализатор,
который эффективно конвертирует толуол в полезные интермедиаты
промышленного органического синтеза в ходе гораздо более экологически
безопасного процесса, чем существующие ныне методы. Возможно, что в
будущем новая методика сможет быть использована в промышленности.
Исследователи из группы Грэма Хатчинса (Graham Hutchings) из Университета Кардиффа разработали процесс конверсии толуола в бензиловый эфир бензойной кислоты. Новый процесс катализируется наночастицами из золото-палладиевого сплава, нанесенными на подложку из углерода (Au-Pd/C) или оксида титана (Au-Pd/TiO2).
Реакция, протекающая в мягких условиях и без растворителя, отличается
высокой селективностью и позволяет получать бензиловый эфир бензойной
кислоты с выходом 95%.
Бензиловый эфир бензойной кислоты представляет собой интермедиат различных химических процессов, он может применяться в фармацевтике, для производства растворителей, пластификаторов и парфюмерных изделий.
Однако, существующие методы получения этого соединения осложняются
использованием реагентов, наносящих вред окружающей среде или низкими
выходами целевого продукта.
Получение коллоидных частиц размером 3–4 нм, содержащих одновременно
золото и платину, с последующим их нанесением на углерод или оксид
титана позволило исследователям получить модифицированную версию
палладий-золотого катализатора, старые модификации которого уже
зарекомендовали себя как катализаторы окислительных процессов.
Хатчинс поясняет, что обычные катализаторы на основе системы Au-Pd содержат наночастицы с размером 6–20 нм, однако
именно уменьшение их размера является ключом для успешного
синтеза бензилбензоата с помощью нового способа. Исследователь
поясняет, что в его группе получен первый гетерогенный катализатор на
основе наночастиц, который сочетает высокие выходы целевого продукта с
эффективной активацией связи C-H и хорошей селективностью.
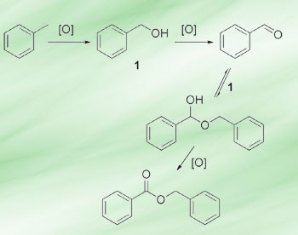
Исследователями предлагается следующий механизм реализации
каталитического цикла – в результате окисления толуола на катализаторе
образуются бензиловый спирт, который окисляется до
бензальдегида. Бензальдегид реагирует с бензиловым спиртом с
образованием гемиацеталя, который затем и окисляется до бензилбензоата,
практически не образуя побочных продуктов.
Исследователи также обнаружили, что твердая подложка, на которую наносится катализатор,
также оказывает влияние на протекание каталитической реакции. Так,
активность системы Au-Pd/C почти в два раза выше в сравнении с системой
Au-Pd/TiO2, при этом исследователям удалось выяснить причины
различия активности, проведя исследование его морфологии с помощью
электронной микроскопии.
Было обнаружено, что наночастицы Au-Pd на подложке из TiO2
образуют большие участки с практически идеально плоской поверхностью, в
то время как наночастицы на углеродной подложке образуют менее
упорядоченную поверхность, содержащую большое число граней, и дефектов
поверхности. Различную активность двух каталитических систем можно
объяснить, предположив, что эти грани являются активными центрами, на
которых протекают каталитические процессы.
Пожалуйста, оцените статью:
- Источник(и):
1. chemport.ru
http://www.nanonewsnet.ru/news/2011/chem-menshe-nanochastitsy-tem-bolshe-vykhod-reaktsii
| 








